npj Aging | (2025) 11:59.
doi.org
Immunometabolism and oxidative stress: roles and therapeutic strategies in cancer and aging
Nan-jie Zhou, Wei-Qian Bao, Cui-fen Zhang, Meng-Lin Jiang, Tu-Liang Liang, Gang-Yuan Ma, Liang Liu , Hu-Dan Pan, Run-Ze Li
Метаболические процессы в иммунной системе и окислительный стресс: роли и терапевтические стратегии при раке и старении
Введение
Иммунометаболизм относится к метаболическим процессам и молекулярной регуляции, вовлеченным в иммунную систему, и играют решающую роль в регуляции развития, активности и функционирования иммунных клеток. Он включает в себя различные аспекты, в том числе выработку энергии, транспорт веществ, передачу сигналов и молекулярную регуляцию, необходимые для поддержания нормальных функций иммунных клеток. К ключевым процессам относят: метаболизм глюкозы (иммунные клетки, особенно Т-клетки и макрофаги, сильно зависят от глюкозы). Регулирование метаболизма липидов имеет решающее значение для функционирования иммунных клеток, метаболизма аминокислот (определенные аминокислоты, такие как глутамат, аргинин, цистеин и т. д., играют важную роль в противоопухолевых, антивозрастных, антиоксидантных и противоинфекционных реакциях).
Биохимические реакции в метаболизме тесно связаны с окислительно-восстановительными реакциями. В биологических системах окислительно-восстановительные реакции происходят посредством переноса электронов от восстановленных молекул-доноров (включая NADPH и тиолы в восстановленном глутатионе (GSH) и аминокислоту цистеин, содержащуюся во многих белках) к молекулам-акцепторам (таким как NADP+ и дисульфидные связи в цистеине, окисленной димерной форме цистеина). Во время окислительного фосфорилирования (OXPHOS) цепь переноса электронов (ETC) доставляет электроны к молекулярному кислороду – процесс, который стимулирует выработку энергии в митохондриях аэробных организмов. Этот процесс неизбежно генерирует радикалы кислорода (также известные как активные формы кислорода (ROS), такие как перекись водорода и супероксид). Поскольку радикалы могут вызывать повреждение ДНК, белков и липидов, аэробные организмы выработали сложные антиоксидантные системы, такие как тиоредоксин (TRX), GSH и система фактора 2, связанного с NF-E2 (NRF2), для балансировки уровней оксидантов в каждой клетке и поддержания окислительно-восстановительного гомеостаза.
Нормальный иммунометаболизм часто сопровождается окислительно-восстановительными реакциями, но когда баланс между окислением и антиоксидантной защитой нарушается, возникает окислительный стресс (ОС). ОС – это состояние дисбаланса между окислением и антиоксидантной защитой в организме, что приводит к воспалительной инфильтрации нейтрофилов, повышенной секреции протеазы и выработке большого количества окислительных промежуточных продуктов. ОС – это негативный эффект, вызванный образованием свободных радикалов в организме, и является существенным фактором, способствующим старению и болезням. В иммунометаболизме ROS могут повреждать липиды, нуклеиновые кислоты и белки, изменяя их функции. Когда баланс между выработкой ROS и антиоксидантной защитой нарушается, возникает окислительный стресс, приводящий к различным заболеваниям.
В этом обзоре основное внимание уделено взаимодействию и регуляторным механизмам между иммунометаболизмом и окислительным стрессом в исследованиях старения и развития опухолей, а также обобщению существующих отчетов о вмешательстве активных компонентов традиционной китайской медицины (рис. 1 ).
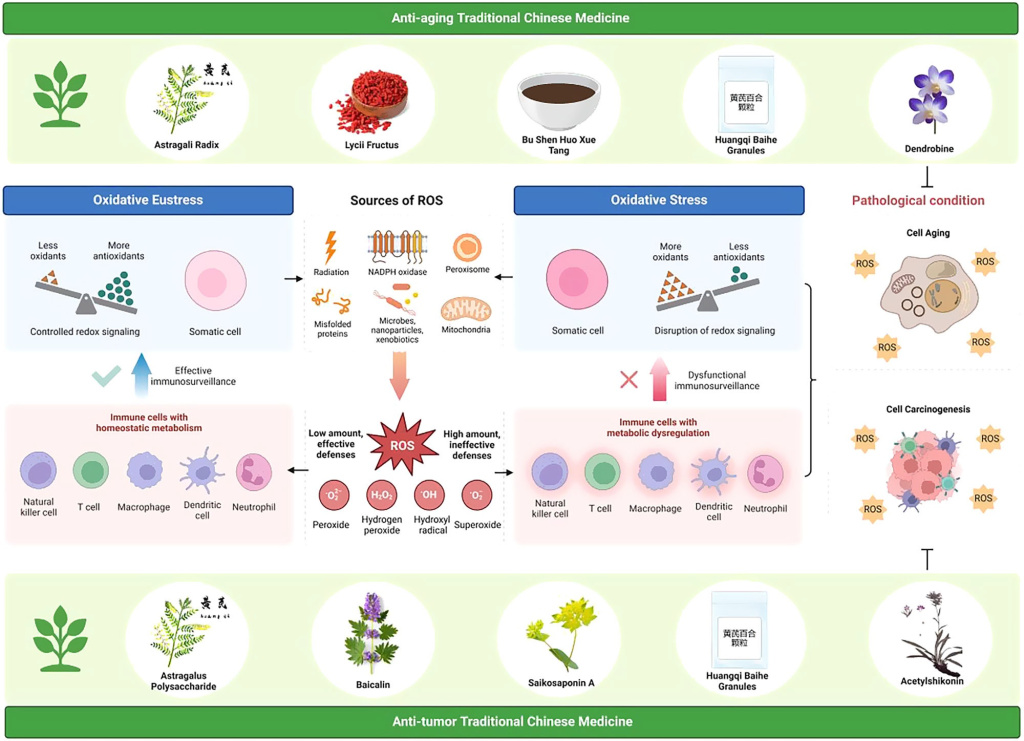 Рисунок 1. Связь окислительного стресса и иммунометаболизма как общая ось старения и образования опухолей, а также ее терапевтическое воздействие в традиционной китайской медицине (ТКМ)
Рисунок 1. Связь окислительного стресса и иммунометаболизма как общая ось старения и образования опухолей, а также ее терапевтическое воздействие в традиционной китайской медицине (ТКМ)
Эта схема объясняет механистическую конвергенцию окислительного стресса и иммунометаболической дисрегуляции в патогенезе старения и рака, наряду с вмешательствами ТКМ, связывающими оба заболевания. Верхняя панель иллюстрирует антивозрастные формулы ТКМ (например, Astragali Radix, Lycii Fructus), в то время как нижняя панель выделяет противоопухолевые агенты ТКМ (например, полисахариды астрагала, байкалин) с перекрывающимися компонентами (например, соединения, полученные из Astragali Radix), подчеркивая их двойной терапевтический потенциал. Физиологический окислительно-восстановительный баланс (слева): контролируемый окислительный эустресс (равновесие ROS/антиоксидантов) поддерживает окислительно-восстановительную сигнализацию и иммунометаболический гомеостаз во врожденных/адаптивных иммунных клетках (NK-клетки, Т-клетки, макрофаги). Это обеспечивает эффективный иммунный надзор за поврежденными или трансформированными клетками посредством сбалансированного гликолиза и митохондриального дыхания. Источники ROS (в центре): митохондриальная дисфункция, НАДФН-оксидазы и ксенобиотики генерируют подтипы ROS (например, O 2− , H 2 O 2 ), которые нарушают окислительно-восстановительную сигнализацию. В частности, связанный со старением распад митохондрий и вызванный раком эффект Варбурга синергически усиливают выработку ROS. Патологические перекрестные помехи (справа): устойчивый окислительный стресс запускает порочный круг: иммунометаболический паралич: избыток ROS ухудшает метаболическую адаптацию иммунных клеток (например, подавление использования глюкозы, дефектное окисление липидов), что ставит под угрозу цитотоксическую активность и презентацию антигена. Коллапс окислительно-восстановительной сигнализации: нерегулируемые окислительно-восстановительные сети истощают антиоксидантную защиту (например, SOD, CAT), одновременно усиливая высвобождение провоспалительных цитокинов, способствуя хроническому воспалительному микроокружению. Конвергенция заболеваний: эта двойная неудача обеспечивает выживание клеток, поврежденных окислительно-восстановительным процессом, что приводит к накоплению стареющих клеток и расширению злокачественных клонов за счет окислительного повреждения ДНК и нарушенных механизмов восстановления, тем самым ускоряя как старение тканей, так и прогрессирование опухолей. Антивозрастные вмешательства (вверху): классические формулы (например, Astragali Radix, Lycii Fructus) смягчают возрастные патологии, модулируя окислительный стресс-иммунометаболические перекрестные помехи, в частности, посредством митохондриальной регуляции ROS и метаболического перепрограммирования стареющих иммунных клеток. Антивозрастные вмешательства (внизу): формулы с растительными комбинациями (например, отвар Bu Shen Huo Xue) и биоактивные соединения (например, Baicalin) противодействуют прогрессированию опухолей за счет двойной регуляции окислительно-восстановительного гомеостаза и иммунометаболической перестройки в иммунных клетках, связанных с опухолью. Терапевтические преимущества ТКМ: ТКМ использует общие компоненты (например, корень астрагала, гранулы Хуанци Байхэ) для одновременного смягчения окислительного повреждения в стареющих тканях и микросреде опухоли посредством регуляции окислительно-восстановительного гомеостаза, омоложения иммунометаболической функции. Эта синергическая стратегия позиционирует TКM как уникальную парадигму для управления сопутствующими заболеваниями, связанными со старением, и раком, особенно у пожилых пациентов с возрастными злокачественными новообразованиями.
Заключение
В этой статье представлен всесторонний обзор основной роли иммунометаболизма и окислительного стресса в развитии рака и старении, а также их взаимодействия. Иммунометаболизм включает метаболические процессы в иммунных клетках, в том числе метаболизм глюкозы, липидов и аминокислот, которые необходимы для поддержания нормальной функции иммунных клеток. Окислительный стресс возникает, когда баланс между прооксидантами и антиоксидантами в организме нарушается, что приводит к перепроизводству ROS, вызывая повреждение клеточных компонентов. В микроокружении опухоли раковые клетки подвергаются метаболическому перепрограммированию для удовлетворения потребностей быстрой пролиферации, процесса, который влияет на функцию иммунных клеток, в частности, посредством влияния на поляризацию ассоциированных с опухолью макрофагов (ТАМ), тем самым способствуя защите опухоли от иммунного ответа и ее прогрессированию. Кроме того, окислительный стресс играет важную роль в инициировании и развитии рака, вызывая повреждение ДНК, нарушая механизмы апоптоза и способствуя уклонению от иммунного ответа. В контексте старения изменения в иммунометаболизме приводят к снижению иммунной функции – явлению, известному как иммуносенесценция. Накопление стареющих клеток и выработка SASP еще больше усугубляют воспалительное состояние и окислительный стресс, ускоряя процесс старения. Окислительный стресс также способствует клеточному старению, влияя на окислительно-восстановительное состояние клеток, повреждение ДНК и окисление белков. Традиционная китайская медицина демонстрирует потенциал в модуляции окислительного стресса и иммунометаболизма, при этом различные активные компоненты китайских трав, как доказано, облегчают процесс старения и подавляют рост опухолей за счет своего антиоксидантного и противовоспалительного действия. Эти компоненты модулируют ключевые сигнальные пути и факторы транскрипции, такие как NF-κB, NRF2 и SIRT1, для смягчения окислительного стресса и иммунометаболического дисбаланса. Подводя итог, можно сказать, что механизмы действия иммунометаболизма и окислительного стресса при раке и старении сложны и взаимосвязаны. Регулируя эти процессы, можно разработать новые стратегии для лечения рака и заболеваний, связанных со старением. Дальнейшие исследования должны глубже изучить молекулярные механизмы этих процессов и разработать эффективные терапевтические вмешательства.






