Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения:
Тестостерон – пг/мл.
Дегидроэпиандростерон – нг/мл.
Андростендион – пг/мл.
Кортизол – нг/мл.
Кортизон – нг/мл.
11-дезоксикортизол – пг/мл.
Альдостерон – пг/мл.
Кортикостерон – пг/мл.
Эстрадиол – пг/мл.
Эстрон – пг/мл.
Эстриол – пг/мл.
Прогестерон – пг/мл.
17-гидроксипрогестерон – пг/мл.
Прегненолон – нг/мл.
Референсные значения
| Женщины (18 лет и старше) | Мужчины (18 лет и старше) |
Тестостерон, пг/мл
|
6,0 - 30,0
|
35,0 - 200,0
|
Дегидроэпиандростерон, нг/мл
|
0,030 - 0,150
|
0,04 - 0,17
|
Андростендион, пг/мл
|
18,0 - 100,0
|
25,0 - 120,0
|
Кортизол, нг/мл
|
1,00 - 7,10
|
0,60 - 6,10
|
Кортизон, нг/мл
|
2,60 - 27,65
|
2,82 - 26,35
|
11-дезоксикортизол, пг/мл
|
1,00 - 9,00
|
1,00 - 9,00
|
Альдостерон, пг/мл
|
10,0 - 90,0
|
10,0 - 90,0
|
Кортикостерон, пг/мл
|
3,00 - 15,00
|
3,00 - 15,00
|
Эстрадиол, пг/мл
|
1,00 - 30,00
|
1,00 - 20,00
|
Эстрон, пг/мл
|
10,0 - 120,0
|
4,0 - 50,0
|
Эстриол, пг/мл
|
0,0 - 85,0
|
0,0 - 40,0
|
Прогестерон, пг/мл
|
Фолликуляр. фаза 5,0-20,0
Лютеиновая фаза: 80-200
Овуляторная фаза: 9-58
Постменопауза: 5-34
|
10,0 - 100,0
|
17-гидроксипрогестерон, пг/мл
|
30 - 180
|
30 - 180
|
Прегненолон, нг/мл
|
0,573 - 0,665
|
0,573 - 0,665
|
Примечание
Референсные значения могут зависеть от метода исследования.
Трактовка результатов исследования «Стероидный профиль 13 показателей с определением прегненолона, ВЭЖХ-МС/МС»
Андрогены – стероидные половые гормоны, производимые половыми железами: яичками у мужчин и яичниками у женщин. У обоих полов синтез андрогенов может происходить в клетках сетчатого слоя коры надпочечников. Отвечают за развитие мужских вторичных половых признаков и вирилизацию при их избытке у женщин либо при нарушении их превращения в эстрогены.
Тестостерон – главный андрогенный стероидный гормон. Около 57% тестостерона, поступающего в кровь, связывается с глобулином, связывающим половые стероиды (ГСПС). Эта связь мешает проникновению гормона в андрогенчувствительные клетки, что практически блокирует его андрогенную активность. Остальная часть тестостерона биологически доступна: связанный с альбумином тестостерон (около 40%), свободный тестостерон (примерно 3%). В тканях тестостерон превращается в активную форму 5 альфа-дигидротестостерон.
Возможные состояния, связанные с повышением концентрации тестостерона:
- Раннее половое созревание.
- Гипертиреоз.
- Новообразования яичек, яичников или надпочечников.
- Врожденная гиперплазия коры надпочечников.
- Болезнь и синдром Иценко-Кушинга.
- Синдром поликистозных яичников.
- Адреногенитальный синдром.
- Хромосомный набор XYY.
- Снижение уровня глобулина, связывающего половые гормоны.
- Прием таких препаратов как даназол, дегидроэпиандростерон, финастерин, флутамид, гонадотропин и нафарелин (у мужчин), гозерелин (в первый месяц лечения), левоноргестрел, мифепристон, моклобемид, нилутамид, пероральные контрацептивы и правастатин (у женщин), фенитоин, рифампин, тамоксифен.
Возможные состояния, связанные с понижением концентрации тестостерона:
- Болезнь гипоталамуса или гипофиза.
- Генетические заболевания (синдром Клайнфельтера).
- Нарушение продукции гонадотропных гормонов гипофиза (в т. ч. гиперпролактинемия).
- Недостаточность надпочечников.
- Гипогонадизм.
- Хронический простатит.
- Ожирение (у мужчин).
- Прием таких препаратов, как даназол (в низких дозах), бузерин, карбамазепин, циметидин, циклофосфамид, ципротерон, дексаметазон, гозерелин, кетоконазол, леупролид, левоноргестрел, сульфат магния, метандростенолон, метилпреднизолон, метирапон, нафарелин (у женщин), нандролон, октреотид, пероральные контрацептивы у женщин, правастатин (у мужчин), преднизон, пиридоглютетимид, спиронолактон, станозолол, тетрациклин, тиоридазин, глюкокортикоиды.
Дегидроэпиандростерон (ДГЭА) образуется в надпочечниках. Малая часть (5-6%) имеет гонадное происхождение. ДГЭА – продукт гидроксилирования 17-гидроксипрегненолона. ДГЭА – прогормон в синтезе половых стероидов: андрогенов (андростендиона и тестостерона) и эстрогенов (эстрадиола и эстрона). Проявляет слабые андрогенные свойства (в 15 раз слабее тестостерона). Повышение уровня его экскреции служит важным показателем гиперандрогении надпочечникового генеза. Большая часть гормона конвертируется в дегидроэпиандростерон сульфат.
Возможные состояния, связанные с повышением концентрации дегидроэпиандростерона:
- Вирилизирующая аденома или карцинома надпочечников.
- Эктопические АКТГ-продуцирующие опухоли.
- Дефицит 21-гидроксилазы и 3β-гидроксистероиддегидрогеназы.
- Адреногенитальный синдром.
- Синдром поликистозных яичников.
- Болезнь Кушинга.
- Гирсутизм, акне у женщин.
Возможные состояния, связанные с понижением концентрации дегидроэпиандростерона:
- Гипофункция надпочечников.
- Задержка полового созревания.
- Прием глюкокортикоидов, пероральных контрацептивов.
Андростендион образуется из дегидроэпиандростерона и из 17-гидроксипрогестерона либо в клетках Лейдига яичек, либо в текальных клетках фолликула яичников. Предшественник тестостерона, эстрадиола и эстрона. Обладает слабой андрогенной активностью (до 20% от биологической активности тестостерона).
Возможные состояния, связанные с повышением концентрации андростендиона:
- Синдром поликистозных яичников.
- Новообразования половых желез и надпочечников.
- Синдром Иценко-Кушинга.
- Врожденная гиперплазия коры надпочечников.
- Болезнь Альцгеймера.
- Привычное невынашивание беременности.
Возможные состояния, связанные с понижением концентрации андростендиона:
˗ возрастное снижение половой функции;
˗ серповидно-клеточная анемия;
˗ гипофункция коры надпочечников;
˗ остеопороз.
Глюкокортикоиды – стероидные гормоны, продуцируемые пучковым слоем коры надпочечников из прогестерона и 17-ОН-прогестерона. Обладают мощным противовоспалительным действием, усиливают катаболизм белков, влияют на углеводный обмен, способствуя повышению уровня глюкозы в крови, через стимуляцию процесса глюконеогенеза. Стимулируют процессы липолиза и перераспределение жировой массы, способствуя развитию абдоминального ожирения на фоне хронического стресса. Обладают мощным противовоспалительным действием.
Кортизол – главный глюкокортикоид.
Возможные состояния, связанные с повышением концентрации кортизола:
- Синдром Иценко-Кушинга.
- Болезнь Иценко-Кушинга.
- Дисфункция гипофиза и недостаточная секреция АКТГ (эктопический АКТГ-синдром).
- Новообразования надпочечников.
- Гипертиреоз.
- Синдром поликистозных яичников.
- Ожирение. Гипогликемия.
- Цирроз печени.
- Некомпенсированный сахарный диабет.
- Стресс, затяжная депрессия.
- Прием атропина, АКТГ, кортикотропин-рилизинг-гормона, кортизона, синтетических глюкокортикоидов, эстрогенов, глюкагона, инсерлина, интерферонов (a-2, b, g), интерлейкина-6, опиатов, пероральных контрацептивов, вазопрессина, опиатов.
Возможные состояния, связанные с понижением концентрации кортизола:
- Врожденная недостаточность коры надпочечников.
- Адреногенитальный синдром с гиперплазией надпочечников.
- Дисфункция гипофиза (гипопитуитаризм).
- Болезнь Аддисона.
- Синдром Нельсона.
- Гипотиреоз.
- Системные заболевания и патологии печени (гепатит, цирроз) и билиарного тракта.
- Прием барбитуратов, беклометазона, клонидина, дексаметазона, дезоксикортикостерона, декстроамфетамина, эфедрина, этомидата, кетоконазола, леводопы, сульфата магния, мидазолама, метилпреднизолона, морфина, окиси азота, препаратов лития, триамцинолона (при длительном лечении).
Кортизон – неактивный метаболит кортизола. Вырабатывается в пучковой зоне коркового вещества надпочечников. Обладает слабой минералокортикоидной активностью. Обеспечивает дополнительную переменную в диагностике различных надпочечниковых расстройств.
Возможные состояния, связанные с повышением концентрации кортизона:
- Болезнь Иценко-Кушинга.
Возможные состояния, связанные с понижением концентрации кортизона:
- Нарушение обменных процессов.
- Болезнь Аддисона.
11-деоксикортизол – непосредственный предшественник кортизола в реакциях стероидогенеза.
Возможные состояния, связанные с повышением концентрации 11-деоксикортизола:
- Врожденная гиперплазия коры надпочечников, вызванная недостаточностью фермента 11β-гидроксилазы.
- Гипоталамическая опухоль.
- Микроаденома гипофиза.
- Апоплексия гипофиза.
- Состояние высокого психоэмоционального и/или физического напряжения.
Возможные состояния, связанные с понижением концентрации 11-деоксикортизола:
- Болезнь Аддисона.
- Адреногенитальный синдром.
- Гипофункция гипофиза.
- Неспецифический инъекционный полиартрит.
- Бронхиальная астма.
Минералокортикоиды – гормоны, синтезируемые в клубочковой зоне коры надпочечников. Ключевые промежуточные минералокортикоиды – предшественники альдостерона: дезоксикортикостерон и кортикостерон, обладающие меньшей минералокортикоидной активностью образуются при участии фермента альдостеронсинтазы и под контролем ангиотензина II. Регулируют электролитный и водный баланс, увеличивая реабсорбцию натрия в дистальных канальцах почек и повышая экскрецию калия с мочой.
Кортикостерон (17-деоксикортизол) – непосредственный предшественник альдостерона.
Возможные состояния, связанные с повышением концентрации кортикостерона:
- Затяжная депрессия, стресс.
- Синдром Иценко-Кушинга.
Возможные состояния, связанные с понижением концентрации кортикостерона:
- Нарушение обменных процессов.
- Болезнь Аддисона.
Альдостерон – главный минералокортикоид, который образуется в клубочковой зоне коры надпочечников при участии фермента альдостеронсинтазы под контролем ренин- ангиотензиновой системы в ответ на снижение объема внеклеточной жидкости. Альдостерон регулирует электролитный и водный баланс, увеличивая реабсорбцию натрия в дистальных канальцах почек и повышая экскрецию калия с мочой.
Возможные состояния, связанные с повышением концентрации альдостерона:
- Цирроз печени.
- Сердечная недостаточность.
- Почечная гипертония.
- Гиперальдостеронизм (синдром Конна).
- Гипергидропексический синдром (синдром Пархона).
- Прием медикаментов, способствующих усилению продукции гормона (эстрогенов, ангиотензина, мочегонных и слабительных средств).
- Диета с низким содержание натриевой соли.
- Беременность.
Возможные состояния, связанные с понижением концентрации альдостерона:
- Хроническая недостаточность коры надпочечников.
- Врожденная гиперплазия надпочечников.
- Болезнь Аддисона.
- Гипоальдостеронизм.
- Нефропатия при сахарном диабете.
- Синдром Тернера.
- Диета с высоким содержание натриевой соли.
Эстрогены – стероидные половые гормоны, преобладающие в женском организме. Синтез эстрогенов у женщин осуществляется фолликулярным аппаратом яичников, а у мужчин – в основном яичками (до 20%). У женщин эстрогены обеспечивают нормальное развитие и функционирование репродуктивной системы, а у мужчин участвуют в регуляции функций простаты и яичек. Эстрогены представлены тремя формами: эстроном (фолликулин) – Е1, эстрадиолом – Е2 и эстриолом – Е3, имеющими разную физиологическую активность: Е2 ˃ Е3 ˃ Е1.
Эстрадиол оказывает мощное феминизирующее влияние на организм, стимулирует развитие влагалища, матки, маточных труб, стромы и протоков молочных желез, формирование вторичных половых признаков по женскому типу, в том числе характерное распределение жировой ткани. Эстрадиол также способствует своевременному отторжению эндометрия и наступлению менструации.
Возможные состояния, связанные с повышением концентрации эстрадиола:
- Избыточная масса тела.
- Гипертиреоз.
- Гиперплазия коры надпочечников.
- Цирроз печени.
- Гинекомастия.
- Эстрогенсекретирующие новообразования яичек или яичников.
- Раннее половое созревание.
- Персистенция фолликула (гиперэстрогения).
- Эндометриоидные кисты яичников.
- Прием таких препаратов, как анаболические стероиды (амиглурацил, метандростенолон, неробол, дианабол, ретаболил), карбамазепин, кломифен (в менопаузе у женщин), кетоконазол, мифепристон, нафарелин, фенитоин, тамоксифен, тролеандромицин, вальпроевая кислота, комбинированные оральные контрацептивы.
Возможные состояния, связанные с понижением концентрации эстрадиола:
- Задержка полового развития.
- Гипогонадизм.
- Гипопитуитаризм.
- Гипотиреоз.
- Дисфункция коры надпочечников.
- Вирильный синдром.
- Менопауза.
- Синдром поликистозных яичников.
- Синдром Шерешевского-Тернера.
- Прием таких препаратов, как аминоглютетимид, препаратов химиотерапии для лечения злокачественных опухолей (гидрея, фторурацил), циметидин, ципротерон, даназол, дексаметазон, эпостан, мегестрол, мифепристон, моклобемид, нафарелин, нандролон, октреотид, правастатин, мини-пили (прогестиновые оральные контрацептивы).
Эстрон (фолликулин) в меньшей степени, чем эстрадиол, участвует в развитии женской репродуктивной системы и регуляции менструального цикла. Вызывает пролиферацию эндометрия, стимулирует развитие матки, фаллопиевых труб, вторичных женских половых признаков, уменьшает климактерические расстройства, влияет на тонус и эластичность урогенитальных структур. В постменопаузальном периоде эстрон преобладает среди эстрогенов, т. к. образуется из андростендиона надпочечников.
Возможные состояния, связанные с повышением концентрации эстрона:
- Избыточная масса тела.
- Гипертиреоз.
- Цирроз печени.
- Новообразования яичников или яичек.
- Новообразования надпочечников.
Возможные состояния, связанные с понижением концентрации эстрона:
- Дисфункция яичников.
- Гипопитуитаризм.
- Синдром Шерешевского-Тернера;
Эстриол (16-гидроксиэстрадиол) – гормон беременности, активно синтезируется плацентой с 25-ой недели. Выработка эстриола напрямую связана с развитием будущего ребенка и отражает состояние фетоплацентарного комплекса. Предшественники эстриола (ДГЭА и 16α-ОН ДГЭА) вырабатываются надпочечниками и печенью плода, после чего поступают в плаценту, где и преобразуются в эстриол. Вне беременности и у мужчин в следовых количествах эстриол синтезируется корой надпочечников.
Возможные состояния, связанные с повышением концентрации эстриола:
- Ожирение.
- Новообразования надпочечников.
- Эстрогенпродуцирующие опухоли яичника.
Возможные состояния, связанные с понижением концентрации эстриола:
- Нарушения у плода (надпочечниковая недостаточность, синдром Дауна, дефект нервной трубки, синдром Эдвардса).
- Резус-конфликт.
- Дисфункция плаценты.
- Пузырный занос.
- Хорионкарцинома.
- Трофобластическая тератома.
- Прием пероральных глюкокортикоидов (преднизолона, бетаметазона), эстрогенов, пенициллина, мепробамата, феназопиридина.
Прогестагены – стероидные половые гормоны, производимые у женщин желтым телом яичников, плацентой и частично корой надпочечников. Прогестагены у женщин обеспечивают возможность наступления и поддержания беременности, регулируя переход слизистой оболочки матки из фазы пролиферации в секреторную фазу и способствуя образованию нормального секреторного эндометрия у женщин. Обладают антиэстрогенными, антианрогенными и антигонадотропными свойствами. У мужчин прогестерон вырабатывается в небольших количествах корой надпочечников и яичками как промежуточный продукт синтеза тестостерона и кортизола, а самостоятельно он принимает участие в работе центральной нервной системы.
Прогестерон – гормон, который синтезируется желтым телом яичников и плацентой из прегненолона под контролем лютеинизирующего гормона. Промежуточный продукт синтеза глюкокортикоидов и альдостерона. Стимулирует секреторную активность эндометрия, влияет на менструальный цикл, течение беременности и развитие плода.
Возможные состояния, связанные с повышением концентрации прогестерона:
- Беременность.
- Текалютеиновые кисты яичника.
- Пузырный занос.
- Новообразования надпочечников и яичек.
- Дисфункциональные маточные кровотечения.
- Дисфункция фетоплацентарного комплекса.
- Замедленное созревание плаценты.
- Почечная недостаточность.
- Врожденная гиперплазия коры надпочечников.
- Нарушение выведения прогестерона при почечной недостаточности.
- Комбинированный дефицит 17α-гидроксилазы/17,20-лиазы.
- Прием таких препаратов, как кломифен, кортикотропин, кетоконазол, мифепристон, прогестерон и его синтетические аналоги, тамоксифен, вальпроевая кислота.
Возможные состояния, связанные с понижением концентрации прогестерона:
- Аменорея.
- Персистенция фолликула (гиперэстрогения).
- Задержка овуляции.
- Ановуляторные дисфункциональные маточные кровотечения (снижение секреции прогестерона во 2-й фазе менструального цикла).
- Воспалительные заболевания внутренних половых органов.
- Нарушение внутриутробного развития плода.
- Угроза прерывания беременности эндокринного генеза.
- Плацентарная недостаточность.
- Прием таких препаратов, как ампициллин, карбамазепин, ципротерон, даназол, эпостан, эстриол, гозерелин, леупромид, пероральные контрацептивы, фенитоин, правастатин, простагландин F2.
17-гидроксипрогестерон (17-ОН прогестерон) – производное прогестерона, малоактивный гормон-предшественник в синтезе эндогенных стероидов: глюкокортикоидов (кортизола), минералокортикоидов (альдостерона), андрогенов и эстрогенов. Лабораторный маркер врожденной дисфункции коры надпочечников и нарушения синтеза эстрогенов в яичниках.
Возможные состояния, связанные с повышением концентрации 17-гидроксипрогестерона:
- Врожденная гиперплазия коры надпочечников.
- Гирсутизм.
- Бесплодие и нарушение менструального цикла.
- Синдром поликистозных яичников.
- Прием некоторых лекарственных препаратов (кортикостероидов и пероральных контрацептивов).
Возможные состояния, связанные с понижением концентрации 17-гидроксипрогестерона:
- Псевдогермафродитизм у мужчин.
Прегненолон является гормоном, синтез которого в организме осуществляется на основе холестерина в надпочечниках. Он играет роль промежуточного звена в реакциях биосинтеза стероидных гормонов: кортизола, альдостерона, половых гормонов (эстрогенов, прогестерона, тестостерона и др.). Этот стероид, первый промежуточный метаболит в цепи синтеза многих стероидных гормонов. Образуется в результате отщепления боковой цепи холестерина. В надпочечниках и гонадах прегненолон трансформируется в 17-ОН-прегненолон или прогестерон и другие метаболиты (см. рис. 1). Содержание прегненолона в циркулирующей крови невысокое, биологическая активность низкая, обычно он рассматривается как предшественник других стероидных гормонов в стероидпродуцирующих клетках надпочечников и гонад, с чем связано основное клиническое применение теста.
Рис. 1. Схема стероидогенеза.
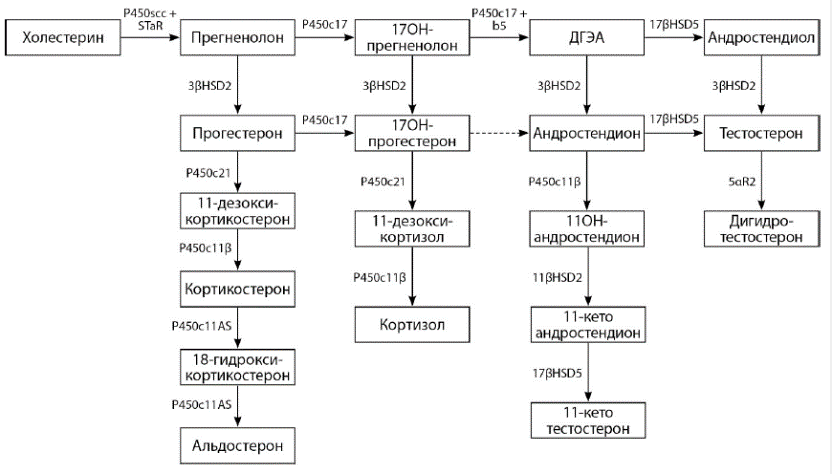
Адреногенитальный синдром (другое название – врожденная гиперплазия коры надпочечников) – это группа наследственных нарушений синтеза стероидных гормонов, возникающих в результате дефицита одного из ключевых ферментов стероидогенеза. На сегодняшний день выявлено несколько мутаций в различных ферментах, приводящих к адреногенитальному синдрому. Дефицит ферментов, участвующих в процессе синтеза кортизола из холестерина, приводит к изменению баланса продуцируемых гормонов. Отмечается снижение продукции глюкокортикоидов и/или минералкортикоидов и повышение содержания промежуточных метаболитов и андрогенов. Снижение уровня кортизола ведет к уменьшению его влияния по механизму отрицательной обратной связи на гипоталамо-гипофизарную систему и дополнительному стимулирующему влиянию АКТГ на надпочечники с увеличением размера желез. Характер дефекта обуславливает клиническую картину разных форм заболеваний этой группы: потенциально опасные для жизни состояния при сольтеряющей форме ВДКН, вирилизация, аменорея, бесплодие у женщин, недостаточная вирилизация у мужчин, преждевременное половое созревание, гирсутизм, олигоменорея, тяжелая угревая сыпь и малозаметные проявления при других формах (8% случаев), к более редким формам относится дефицит 3-бета-гидроксистероиддегидрогеназы (менее 5% случаев), 17-альфа-гидроксилазы, дефект гена StAR и пр.
Оценка изменения содержания стероидных гормонов и их промежуточных метаболитов, к которым относится и прегненолон, используется в диагностике различных форм врожденной дисфункции коры надпочечников.
Наибольшее клиническое значение имеют следующие ферментопатии:
- дефицит 21-гидроксилазы (самая частая форма, является причиной адреногенитального синдрома в 90% случаев);
- дефицит 11-бета-гидроксилазы (вторая по частоте форма, 5-8% случаев);
- дефицит 3-бета-гидроксистероиддегидрогеназы (редкая форма, 3-5% случаев);
- дефицит 17-альфа-гидроксилазы и еще более редкие формы.
Таким образом, повышение уровня прегненолона является диагностическим тестом для подтверждения дефицита 3-бета-гидроксистероиддегидрогеназы. Это исследование, однако, редко выполняют отдельно. В большинстве случаев тест на прегненолон выполняют в комплексе с другими стероидными гормонами и их метаболитами. Результат анализа оценивают с учетом всех значимых клинических, лабораторных инструментальных исследований.
Причины повышения: дефицит 3-бета-гидроксистероиддегидрогеназы.
Причины понижения: самостоятельного клинического значения не имеет.
На результат может влиять применение некоторых лекарственных препаратов, например кетоконазола.





