npj Aging | (2025) 11:76.
Modulating biological aging with foodderived signals: a systems and precision nutrition perspective
Carsten Carlberg, Andreas Blüthner, Irini Schoeman-Giziakis, Annemarie Oosting, Luca Cocolin
Старение — это естественный биологический процесс, который затрагивает каждого человека, но по-разному. Хотя старение остановить невозможно, есть все больше данных о том, что его можно контролировать и, в...
npj Aging | (2025) 11:76.
Modulating biological aging with foodderived signals: a systems and precision nutrition perspective
Carsten Carlberg, Andreas Blüthner, Irini Schoeman-Giziakis, Annemarie Oosting, Luca Cocolin
Старение — это естественный биологический процесс, который затрагивает каждого человека, но по-разному. Хотя старение остановить невозможно, есть все больше данных о том, что его можно контролировать и, возможно, обратить вспять, меняя образ жизни и окружающую среду. Среди этих факторов питание является одним из основных факторов, определяющих скорость старения и устойчивость к неинфекционным заболеваниям (НИЗ).
В 2023 году средняя продолжительность жизни в странах Европейского союза составила 81,4 года. Однако эти дополнительные годы не всегда коррелируют с хорошим здоровьем. Такие показатели, как годы здоровой жизни (HLY) и годы жизни с поправкой на инвалидность (DALY), подчеркивают разрыв между долголетием и качеством жизни. В области геронтологии цель здорового старения заключается не только в увеличении продолжительности жизни, но и в максимальном увеличении продолжительности здоровой жизни, то есть количества лет, прожитых в состоянии физического, эмоционального и когнитивного благополучия.
Выбор образа жизни, включая питание, физическую активность, контроль стресса и качество сна, существенно влияет на результаты старения. Однако влияние генетических и эпигенетических факторов, а также микробиома усложняет эту ситуацию. Поскольку исследователи стремятся понять, что отличает тех, кто стареет благополучно, от тех, у кого рано развиваются хронические заболевания, интеграция показателей биологического старения открывает многообещающее направление.
В дополнение к модифицируемым факторам образа жизни, важно признать, что генетический фон также вносит значительный вклад в биологическое старение. Исследования семейного долголетия и когорт долгожителей показывают, что наследственные факторы могут модулировать траектории старения, независимо или совместно с факторами образа жизни. Исследования ассоциаций и секвенирования по всему геному показывают, что долголетие частично наследуется, при этом определенные аллели связаны с более медленным старением или с устойчивостью к болезням. Важно отметить, что эффективность диетических или поведенческих вмешательств может зависеть от генетики человека, что подчеркивает необходимость комплексных подходов, учитывающих как внутренние, так и внешние факторы биологического старения.
Еще одной новой концепцией, лежащей в основе системного питания, является концепция «темной материи» (NDM). Этот термин охватывает обширный пул из более чем 139 000 малых молекул пищевого происхождения, из которых лишь небольшая часть обладает известными биологическими функциями или идентифицированными белковыми мишенями. Эти соединения могут играть ключевую регуляторную роль в путях, связанных со старением, но остаются в значительной степени неизученными. Таким образом, NDM представляет собой новую область для исследований и потенциальный мост между сложными моделями питания и специфическими молекулярными вмешательствами, направленными на модуляцию биологического возраста.
В этой перспективе рассматриваются: i) как режимы питания влияют на биологический возраст посредством молекулярных механизмов; ii) роль микробиома кишечника в обеспечении устойчивости; и iii) как «омика» и искусственный интеллект (ИИ) обеспечивают точное питание для стареющего населения.
Несколько факторов, включая диету, физическую активность и социальные отношения, влияют на старение и развитие неинфекционных заболеваний. Исследования популяций долгожителей показывают, что богатые растительной пищей диеты, сбалансированное потребление энергии и регулярная физическая активность связаны с более низким риском хронических заболеваний и улучшением качества жизни в пожилом возрасте. Эти результаты дополнительно подтверждаются недавними доказательствами двух крупных проспективных когорт в США (исследование здоровья медсестер и последующее исследование медицинских работников), в которых участвовали более 100 000 человек, наблюдавшихся в течение 30 лет. Эти результаты расширяют существующие знания, связывая соблюдение диеты с многодоменными показателями старения, включая когнитивную и метаболическую функцию. Исследования показали, что более строгое соблюдение нескольких диетических моделей, включая AHEI (альтернативный индекс здорового питания), AMED (альтернативный средиземноморский индекс), DASH (диетические подходы к остановке гипертонии) и PHDI (планетарный индекс здорового питания), было тесно связано с повышенными шансами здорового старения. К ним относятся сохранение когнитивных, физических и умственных функций, а также отсутствие хронических заболеваний в пожилом возрасте. Среди этих показателей наиболее выраженную связь продемонстрировал показатель AHEI, почти удвоивший вероятность здорового старения по сравнению с самым низким квинтилем приверженности.
Хотя структурированные модели питания, такие как средиземноморская диета или AHEI, демонстрируют выраженную связь со здоровым старением, их эффекты обусловлены сложным взаимодействием многочисленных биологически активных соединений, содержащихся в пище. Точное воздействие на конкретные молекулярные пути, например, на пути, модулируемые полифенолами, омега-3 жирными кислотами или витамином D3, может улучшить наше понимание механизмов и стратегии вмешательства. Вместо дихотомии «или-или», модели, основанные на комплексном подходе к питанию, и молекулярно-ориентированные модели следует рассматривать как синергетические компоненты единой стратегии здорового старения.
Помимо факторов образа жизни, новые исследования подчеркивают роль биологических маркеров в оценке траекторий старения. Одним из наиболее перспективных инструментов в этой области является использование эпигенетических часов. Эпигенетические факторы, включая иммуномодулирующие микронутриенты, такие как витамин D3, играют важную роль в старении. Они поддерживают иммунитет, уменьшают хроническое воспаление, оптимизируют метаболические пути, включая контроль окислительного стресса, и помогают поддерживать сбалансированный микробиом кишечника, что в совокупности способствует общему здоровью и долголетию. Понимание взаимодействия между образом жизни, социальной средой и генетической предрасположенностью имеет решающее значение для разработки комплексных стратегий поддержки здорового старения как на индивидуальном, так и на популяционном уровне.
Большинство эпигенетических часов полагаются на объемные образцы тканей, такие как кровь, которые содержат различные типы клеток, изменяющиеся с возрастом. Эта гетерогенность может скрывать истинные сигналы старения. Поэтому важно различать внешние часы (на которые влияет состав клеток) и внутренние часы (скорректированные с учетом пропорций типов клеток). Четкое различие между хронологическим и биологическим возрастом имеет важное значение для продвижения исследований старения. Эпигенетические часы, которые оценивают биологический возраст на основе паттернов метилирования ДНК, можно в целом разделить на несколько типов. Это хронологические часы (например, Horvath), которые близко совпадают с фактическим возрастом; биологические часы риска (например, GrimAge), которые предсказывают исходы для здоровья и риск смертности; митотические часы (например, epiTOC2), которые отслеживают клеточную репликацию; и часы шумового барометра, которые фиксируют стохастические вариации в паттернах метилирования. Каждая категория служит различным целям: от оценки риска заболевания до оценки влияния вмешательств, что делает выбор часов критически важным для точной интерпретации траекторий старения. Более того, недавние исследования показывают, что часть дисперсии в скорости эпигенетических часов может быть генетически обусловлена.
Выбор часов должен соответствовать цели исследования. Например, GrimAge особенно хорошо подходит для оценки риска неинфекционных заболеваний и прогнозирования смертности. С момента появления первых эпигенетических часов эта область быстро расширилась, и в настоящее время разработано множество часов с использованием разнообразных алгоритмов и методов обработки данных. Помимо эпигенетики, часы старения также были построены с использованием таксономического профилирования микробиома кишечника, что дает дополнительное представление о старении хозяина. Более того, циркадные ритмы в эпителии кишечника зависят от характера питания и сигналов, получаемых от микробиоты, которые взаимодействуют с иммунной и нервной системами хозяина. Это говорит о том, что поддержание ритмичности во взаимодействиях микробиом-хозяин может быть дополнительной целью для вмешательств, направленных на замедление когнитивного старения. Дополнительная сложность возникает из-за недавних открытий, показывающих, что протеомные сигнатуры плазмы могут определять органоспецифические часы у людей, открывая новые возможности для точной диагностики старения.
На рисунке 1 проиллюстрирована концепция биологического возраста и его отличие от хронологического возраста. Хронологический возраст – это фактический возраст в годах, в то время как биологический возраст отражает, насколько хорошо организм человека функционирует по сравнению с другими людьми того же хронологического возраста. Такие факторы, как генетика, образ жизни и окружающая среда, способствуют этому изменению. На рисунке изображены три гипотетических человека в возрасте 70 лет (обозначены кружками). Несмотря на одинаковый хронологический возраст, их биологический возраст различается. Визуально это представлено тремя различными траекториями:
- оптимальное старение (зеленая линия): биологический возраст этого человека остается ниже хронологического возраста, что отражает хорошее здоровье, сбалансированное питание, регулярную физическую активность и минимум хронических заболеваний;
- недостаточно оптимальное старение (оранжевая линия): у этого человека наблюдается умеренное биологическое старение, возможно, из-за плохих привычек питания или отсутствия физической активности, что приводит к ранним признакам старения и возникновению хронических заболеваний;
- неоптимальное старение (красная линия): биологический возраст этого человека превышает его хронологический возраст, что указывает на ускоренное старение, вероятно, вызванное нездоровым образом жизни, курением или другими формами интоксикации, неправильным питанием, отсутствием физической активности, и повышенный риск возрастных заболеваний, таких как сердечно-сосудистые заболевания или диабет.
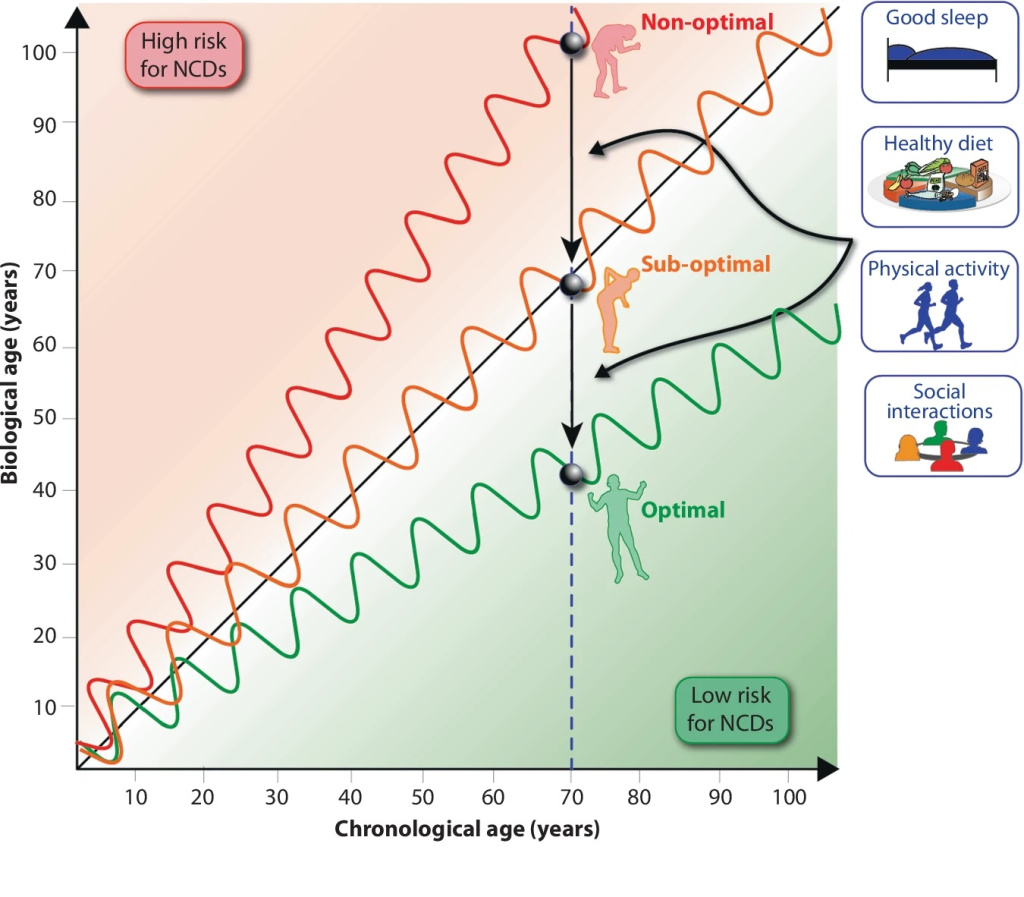 Рисунок 1. Расходящиеся траектории биологического старения и изменяемые вмешательства в образ жизни.
Рисунок 1. Расходящиеся траектории биологического старения и изменяемые вмешательства в образ жизни.
Биологический возраст, в отличие от хронологического, отражает функциональное состояние и риск для здоровья человека. Диагональная пунктирная линия представляет хронологическое старение. Три показательные траектории старения: оптимальная (зеленая), недостаточно оптимальная (оранжевая) и неоптимальная (красная), демонстрируют, как биологический возраст может различаться в зависимости от образа жизни. Люди, стареющие в оптимальном режиме, поддерживают биологический возраст ниже своего хронологического возраста и демонстрируют более низкий риск развития неинфекционных заболеваний, в то время как люди с неоптимальным старением испытывают ускоренное биологическое старение и более высокий риск развития неинфекционных заболеваний. Волновые паттерны отражают краткосрочную изменчивость, обусловленную суточным и сезонными факторами. Стрелки указывают на то, как целенаправленные вмешательства, такие как хороший сон, здоровое питание, регулярная физическая активность и социальная активность, могут замедлить старение и переместить людей в сторону более благоприятной траектории старения.
Это подчеркивает роль образа жизни в формировании биологического старения, при этом диета, физические упражнения, качество сна и социальное взаимодействие являются ключевыми факторами поддержания здоровья и замедления биологического старения. Эта концепция критически важна для понимания того, как мы можем вмешаться, чтобы замедлить старение и предотвратить хронические заболевания. Питание является важным фактором, влияющим на биологический возраст. Сбалансированное питание, богатое питательными веществами, такими как антиоксиданты, клетчатка и полиненасыщенные жиры, такие как омега-3 жирные кислоты, может помочь замедлить прогрессирование старения. И наоборот, неправильное питание, такое как высокое содержание сахара, трансжиров, и низкое содержание клетчатки, ускоряет процесс старения, увеличивая риск развития неинфекционных заболеваний.
Растительная диета, содержащая высококачественный белок, связана с 15%-ным снижением риска сердечно-сосудистых заболеваний и 21%-ным снижением риска ишемической болезни сердца. Механистически это связано с такими путями, как ингибирование mTOR (мишень рапамицина у млекопитающих), модуляция сиртуинов и снижение окислительного стресса. Более того, соблюдение средиземноморской диеты связано с уменьшением воспаления и улучшением когнитивной функции, причем исследования указывают на более низкий риск снижения когнитивных способностей и деменции среди ее приверженцев. Было показано, что веганские диеты улучшают гликемию и контроль веса у людей с диабетом 2-го типа. Однако в растительных диетах может не хватать необходимых микронутриентов, таких как витамин B12, витамин D3, железо, кальций и длинноцепочечные омега-3 жирные кислоты. Обеспечение их адекватного потребления путем тщательного планирования диеты или приема добавок имеет важное значение.
Более того, поддержание здорового веса посредством сбалансированного питания и регулярных физических упражнений может предотвратить или отсрочить развитие многих хронических заболеваний, таких как гипертония, диабет и сердечно-сосудистые заболевания. Интересно, что социальная активность и крепкие семейные связи, как это наблюдается у жителей «голубой зоны», также значительно способствуют долголетию и общему благополучию. В отличие от этого, одиночество связано с ухудшением качества питания, что повышает риск недоедания.
Бактерии кишечника человека эволюционировали совместно со своими хозяевами на протяжении миллионов лет, достигнув уровня адаптации, значительно превосходящего уровень большинства патогенов. Однако изменения в питании и окружающей среде, произошедшие после промышленной революции, оказали новое селективное давление как на геном человека, так и на микробиом кишечника. Благодаря короткому периоду генерации микробы адаптировались быстрее, что привело к выраженной межиндивидуальной изменчивости состава микробиома, определяемого питанием, возрастом, полом, географией и состоянием здоровья.
Кишечный микробиом играет важнейшую роль в развитии и поддержании иммунитета и метаболической активности на протяжении всей жизни. Он развивается с момента ранней колонизации при рождении, диверсифицируется в зависимости от питания и полового созревания и стабилизируется, формируя уникальный профиль взрослого человека. Старение нарушает этот баланс, увеличивая изменчивость и обилие таких таксонов, как Bacteroides и Alistipes, под влиянием факторов питания и образа жизни на протяжении всей жизни.
Здоровье человека можно активно формировать, модулируя микробиом через диету и более широкие методы производства продуктов питания. Такие диеты, как средиземноморская, связаны с микробными профилями, защищающими от рака, связанного с ожирением. Хотя универсального «здорового микробиома» не существует, некоторые таксоны (например, Faecalibacterium) связаны с пользой для здоровья и более низким эпигенетическим возрастом, в то время как другие (например, Ruminococcus) связаны с дисбактериозом и более высоким риском неинфекционных заболеваний. Ключевым механизмом, лежащим в основе этого, является продукция провоспалительных молекул, которые стимулируют системное воспаление и прогрессирование заболевания (рис. 2А). Однако часы, основанные на микробиоме, остаются популяционно-специфичными и нуждаются в дальнейшей кросс-когортной валидации.
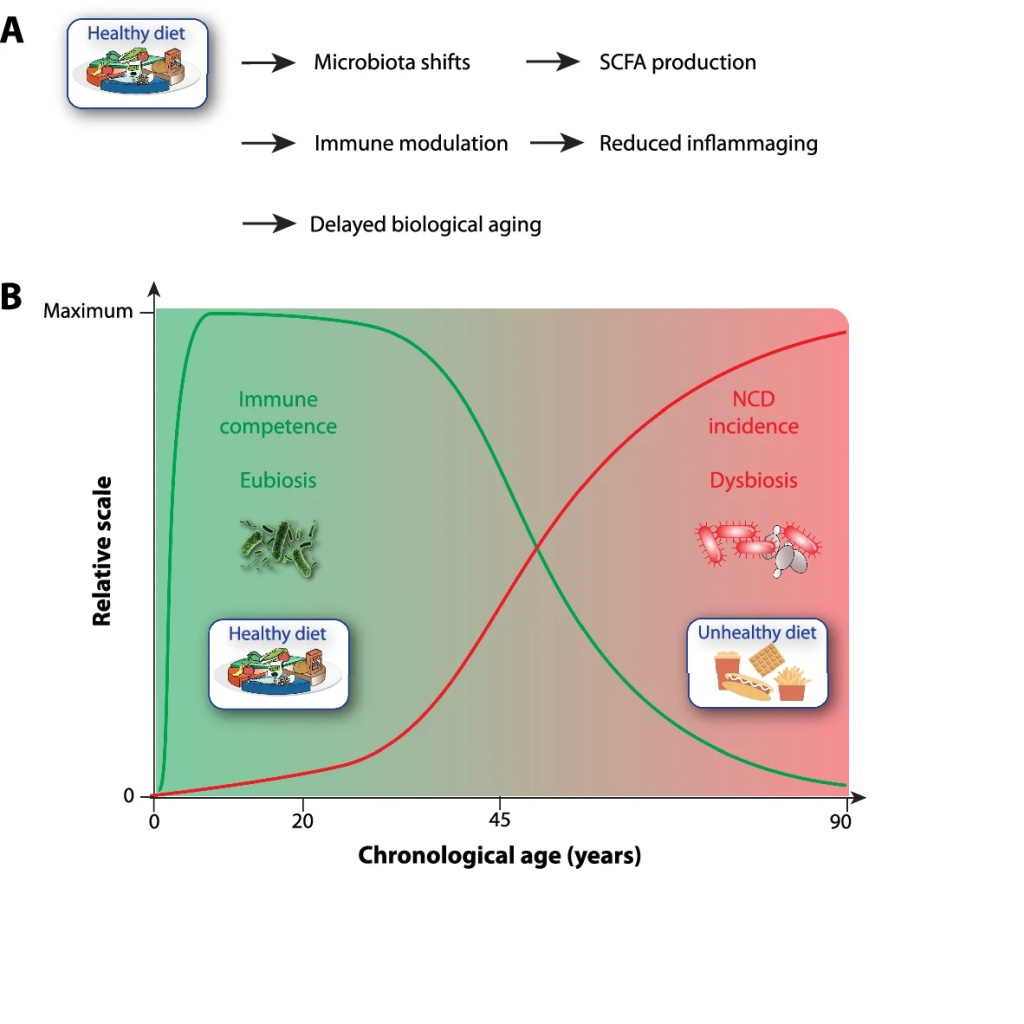 Рисунок 2. Влияние диеты на микробиом кишечника, иммуннитет и биологическое старение.
Рисунок 2. Влияние диеты на микробиом кишечника, иммуннитет и биологическое старение.
A – здоровое питание способствует полезным сдвигам в микробиоте, которые усиливают выработку короткоцепочечных жирных кислот (SCFA), модулируют иммунные реакции и уменьшают хроническое слабовыраженное воспаление («инфламмейджинг»). Эти эффекты в совокупности способствуют замедлению биологического старения. B – схематический обзор возрастных траекторий иммунной компетентности и заболеваемости НИЗ в связи с качеством питания. Соблюдение здорового питания в раннем возрасте поддерживает эубиоз и крепкую иммунную функцию (зеленая кривая), тогда как нездоровое питание связано с дисбактериозом, усилением воспаления и ростом бремени НИЗ с течением времени (красная кривая). Переходная зона отражает уязвимость среднего возраста, когда диетический выбор критически формирует траектории старения. Иллюстративные значки отображают примеры здорового (например, богатые клетчаткой растительные продукты, ферментированные продукты) и нездорового (например, обработанное мясо, сладости) рациона питания.
Пища не только насыщает, но и является топливом для кишечных микробов. Высококачественные диетические модели, особенно те, которые богаты клетчаткой, полиненасыщенными жирами и растительными продуктами, надежно связаны с улучшенными системными результатами старения. Определенные диетические компоненты, такие как орехи, бобовые, нежирные молочные продукты и ненасыщенные жиры, положительно связаны с несколькими областями здорового старения. Таким образом, диета играет центральную роль в формировании микробного состава и активности. Долгосрочные диеты с высоким содержанием животных жиров и белков связаны с воспалением, тогда как богатые клетчаткой растительные диеты усиливают выработку противовоспалительных короткоцепочечных жирных кислот. Поэтому питание, ориентированное на микробиом, имеет решающее значение для укрепления иммунного здоровья и снижения риска НИЗ на протяжении всей жизни (рис. 2В).
Аутофагическое очищение от бактериальных токсинов, поврежденных органелл и неправильно свернувшихся белков с возрастом значительно снижается. Это снижение способствует возникновению порочного круга: хроническое воспаление кишечника нарушает аутофагию, что, в свою очередь, усугубляет воспаление и способствует дисбактериозу. Поэтому для восстановления и поддержания здорового баланса аутофагии критически важны пищевые вмешательства.
Профилактика дисбактериоза, или активное изменение микробиома кишечника, становится ключевой стратегией содействия здоровому старению. Например, трансплантация микробиоты открывает возможность переноса микробных профилей, связанных с долголетием, что имеет многообещающие перспективы даже в контексте нейродегенеративных заболеваний.
Более того, кишечник служит центральным узлом нейроиммунной коммуникации. Ранние исследования оси «кишечник – мозг» подчеркивали роль микробных метаболитов в передаче сигналов в центральную нервную систему, однако недавние исследования выявили прямое взаимодействие между кишечной микрофлорой и периферическими нейронами. Эти данные подтверждают идею о том, что диетическая модуляция микробиома может оказывать защитное действие против нейродегенеративных заболеваний, таких как болезнь Альцгеймера и Паркинсона. Стратегии здорового старения, основанные на правильном питании, включая междисциплинарное и межсекторальное сотрудничество, обещают отсрочить или предотвратить деменцию.
В то же время, возрастные нарушения связи циркадных часов, особенно между центральными часами супрахиазматического ядра и периферическими тканями, связывают с физиологическим упадком. Эти нарушения влияют на гормональную регуляцию (например, мелатонин, кортизол), иммунные реакции, метаболические ритмы и когнитивные функции. Такие вмешательства, как светотерапия и гигиена сна, могут помочь ресинхронизировать циркадные ритмы и восстановить системный баланс.
Важно отметить, что циркадные ритмы в эпителии кишечника формируются под влиянием особенностей питания и сигналов, поступающих от микробиоты, которые взаимодействуют с иммунной и нервной системами хозяина. Таким образом, поддержание ритмичности взаимодействия микробиома и хозяина может служить дополнительной целью для замедления когнитивного старения. Ограниченное по времени питание, согласующее потребление питательных веществ с внутренними циркадными ритмами, представляет собой мощный метод восстановления ритмичности в периферических тканях.
Для полной реализации этих возможностей крайне необходимо выявить надежные биомаркеры, связывающие состав микробиома с воспалительным статусом. Такие маркеры позволят проводить ранние целенаправленные вмешательства для снижения риска неинфекционных заболеваний.
Недавние достижения в области часов старения предоставляют детальную основу для применения оценок биологического возраста к стратегиям питания и здоровья. Эти технологии позволяют исследователям отслеживать биомаркеры старения и определять вмешательства, которые могут замедлить биологическое старение. Консорциум по биомаркерам старения (www.agingconsortium.org ) предлагает комплексную основу для оценки биологических биомаркеров старения по шести критическим параметрам: осуществимость, валидность, механизм, обобщаемость, восприимчивость и стоимость. Эти критерии имеют решающее значение для определения того, могут ли биомаркеры превратиться из исследовательских инструментов в практические в клинических условиях и условиях общественного здравоохранения. Подчеркивание восприимчивости к вмешательствам, прогностической валидности в отношении множественных возрастных заболеваний и надежной кросс-популяционной валидации повышает их трансляционную ценность.
Омические технологии также открыли путь к точному питанию, позволяющему адаптировать рацион питания к молекулярному профилю человека, включая генетику, эпигенетику, метаболомику, липидомику и метагеномику, что позволяет разрабатывать более эффективные стратегии для поддержания здорового старения. Например, исследования показали, что биоактивные питательные вещества и ряд пищевых компонентов, таких как витамин D3, полифенолы и омега-3 жирные кислоты, могут модулировать воспалительные процессы и улучшать метаболическую функцию, что может способствовать профилактике хронических заболеваний, связанных со старением.
Чтобы в полной мере раскрыть потенциал прецизионных методов лечения старения, крайне важно расширить наше понимание биохимии питания за пределы общеизвестных нутриентов. Как уже упоминалось, концепция NDM относится к практически неизученному аспекту малых молекул пищевого происхождения, многие из которых не имеют известных белковых мишеней, но могут оказывать регуляторное влияние на ключевые пути старения. Эта химическая сложность сопоставима со сложностью фармацевтических библиотек и включает молекулы, способные модулировать почти половину протеома человека. Интеграция NDM в системную биологию обладает большим потенциалом для выявления новых пищевых соединений, влияющих на биологическое старение. Например, профилирование NDM ферментированных продуктов может выявить сенотерапевтические производные полифенолов. Приоритизация целей NDM с помощью омиксных данных и часов старения поможет превратить эти открытия в действенные нутритивные вмешательства.
Новые подходы к машинному обучению, в частности, модели глубокого обучения, такие как AltumAge или DeepMAge предлагают мощные инструменты для выявления сложных нелинейных взаимосвязей между эпигенетическими маркерами старения и интеграции разнообразных мультиомных наборов данных. В сочетании с объяснимыми методами искусственного интеллекта, такими как SHAP (Shapley Additive Explanations), эти модели дают интерпретируемую информацию о том, как конкретные особенности метилирования ДНК влияют на прогнозы биологического возраста. Что особенно важно, они также могут помочь выявить эпигенетические локусы, реагирующие на образ жизни или диетические вмешательства, тем самым способствуя разработке точных стратегий питания.
В более широком смысле, интеграция ИИ в исследования старения расширяет наши возможности по выявлению закономерностей в больших наборах данных, прогнозированию последствий для здоровья и разработке более целенаправленных вмешательств для стареющего населения. Например, уже разработано несколько часов старения на основе микробиома. Было показано, что специфические микробные сигнатуры коррелируют со здоровым старением и даже предсказывают выживаемость. Это говорит о том, что модели на основе ИИ также могут быть полезны для оценки эффективности точного питания с целью продления жизни.
Несмотря на их многообещающие результаты, интерпретация биомаркеров старения пока остается ограниченной. Нелинейные траектории многих молекулярных маркеров на протяжении жизни усложняют ситуацию. Для их интеграции в здравоохранение и персонализированные профилактические стратегии необходимы дополнительные усилия по валидации этих биомаркеров и обеспечению их интерпретируемости и применимости в реальных клинических условиях.
- Биомаркеры старения должны быть проверены в различных группах населения и поддаваться модифицируемым вмешательствам.
- Биомаркеры должны стать экономически эффективными, интерпретируемыми и клинически применимыми, особенно при использовании в качестве инструментов скрининга или реагирования в персонализированном питании и профилактической медицине.
- Исследования внедрения должны связывать биомаркеры с результатами, которые влияют на то, как люди «чувствуют себя, функционируют и выживают».
Рекомендуется поэтапная интеграция в клинические исследования (например, для стратификации участников испытаний), а затем в практику (например, для разработки программ коррекции образа жизни или испытаний геропротекторов). Цифровые инструменты для здоровья и носимые датчики могут помочь отслеживать изменения, связанные с биомаркерами, с течением времени и создавать персонализированные профили старения.
Синонимы: Длина теломер; Клеточное старение; Укорочение хромосом. Краткое описание исследования «Генетическая диагностика клеточного старения (измерение длины теломер)» Теломеры – это концевые участки хромосом, защищающие ДНК в процессе репликативного дел...
Синонимы: Анализ буккального соскоба «MyExpert» My Genetics. Genetic panel «MyExpert» My Genetics; Gene panel testing «MyExpert» My Genetics. Краткое описание исследования «Генетическая панель MyExpert» Генетическая панель «MyExpert» My Ge...
Перевод на русский язык научной статьи осуществлен в соответствии с условиями открытой лицензии Creative Commons Attributions (CC BY) (Creative Commons — Attribution 4.0 International — CC BY 4.0)





